【综述】Masquelet技术重建骨缺损研究进展
文章来源:中华骨科杂志, 2018,38(21) : 1330-1336
作者:袁昊龙 王志刚 张锴
摘要
导致骨缺损的原因很多,包括外伤、恶性肿瘤切除、慢性骨髓炎和先天性因素等。骨缺损的治疗技术包括自体骨松质骨植骨技术、带血管腓骨移植技术、骨搬移技术、Masquelet技术等。膜诱导技术由Masquelet等在1986年首次发现,该技术为治疗大段骨缺损提供了一种简单、安全的方案。Masquelet技术治疗骨缺损主要分两个阶段,第一阶段包括创面彻底清创、保持骨折端的稳定、放置骨水泥、无张力关闭创面;待6~8周后,行第二阶段手术,即切开诱导膜,取出骨水泥后植骨。骨水泥可选择聚甲基丙烯酸甲酯(PMMA),也可选择磷酸钙、硫酸钙等其他材料,必要时可结合抗生素同时使用。不同的骨水泥诱导的生物膜也各具特点。诱导膜能够分泌转化生长因子-β1、骨形态发生蛋白-2、血小板内皮细胞黏附分子和血管内皮生长因子等多种成骨生长因子、血管生成相关因子,并形成一个独立的空间,将缺损内部的植骨与外界环境隔离,避免了骨移植后植骨吸收的现象,为骨缺损愈合提供了稳定的生物学环境。Masquelet技术操作简单、安全、并发症少、对受区要求低、易于被患者接受和临床推广,适用于各部位骨缺损,特别是其他治疗方法无效的大段骨缺损治疗。
骨缺损的定义为骨缺损部位无新生骨形成或形成的新生骨长度小于缺损面积的10%,缺损长度一般为直径的2~3倍[1],常见于创伤、恶性肿瘤切除后、慢性骨髓炎和先天性骨缺损。骨缺损的治疗技术包括自体骨松质骨植骨技术、带血管腓骨移植技术、骨搬移技术、Masquelet技术等,治疗方案各有优缺点。膜诱导技术由Masquelet等在1986年首次发现,并于2000年报告应用膜诱导成功治疗35例长骨骨干缺损,缺损范围为4~25 cm[2]。此后,人们将该技术称为Masquelet技术。
Masquelet技术治疗骨缺损分两个阶段。第一阶段:彻底清创,必要时行皮瓣转移,闭合创面,然后在骨缺损区以聚甲基丙烯酸甲酯(PMMA)骨水泥填充塑形。第二阶段:第一阶段6~8周后,若感染控制、软组织愈合良好,去除缺损部位骨水泥,保留形成的生物膜结构,然后在膜内填充颗粒状自体松质骨[3]。本文将对Masquelet技术的应用及影响因素等做一综述,为临床应用Masquelet技术治疗骨缺损提供理论指导。
本文以'骨缺损' 、'诱导膜' 、'Masquelet技术' 、'bone defect' 、'induced membrane' 、'Masquelet' 、'antibiotic cement spacer'等作为关键词,在中国知网、万方、PubMed、Springer数据库中进行检索,筛选自2000年1月1日至2017年6月1日的文献。文献纳入标准:①Masquelet技术在骨科疾病的应用;②Masquelet技术的分子生物学机制;③Masquelet技术在骨科疾病应用的进展。排除标准:①无法获得全文的文献;②与研究主题不相关的文献;③重复的文献;④非中英文文献。共查阅文献1 049篇,依据纳入及排除标准,最终纳入文献49篇,其中中文文献9篇,英文文献40篇(图1)。
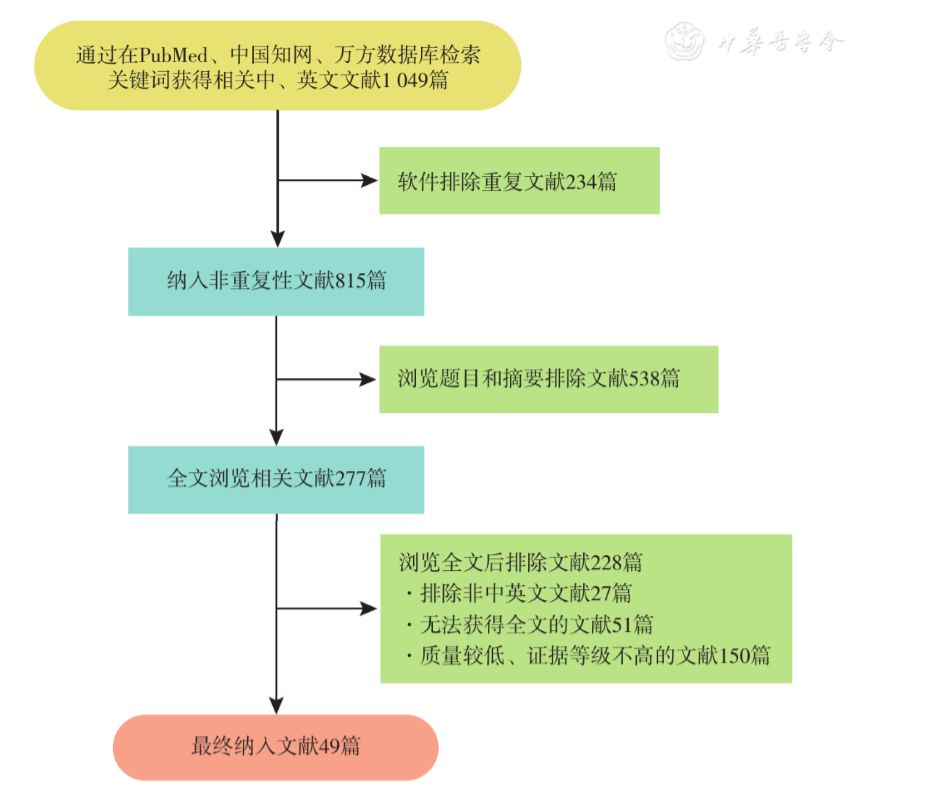
图1 文献筛选流程图
一、Masquelet技术的临床应用
(一)创伤性骨缺损
Flamans等[4]利用Masquelet技术治疗11例手部及腕部创伤性骨缺损,随访4个月后,骨愈合率达82%,无一例出现其他并发症。Apard等[5]利用Masquelet技术治疗12例由外伤引起的骨缺损;一期采用髓内钉内固定,二期植骨,术后4个月愈合率达91.6%。Wong等[6]报告Masquelet技术治疗9例由外伤导致的骨缺损,缺损部位包括尺骨鹰嘴、肱骨、胫骨,缺损长度为2~8 cm,两次手术间隔时间平均为48.5 d,所有骨折均愈合且无一例发生并发症。许多临床研究表明,Masquelet技术治疗四肢创伤后骨缺损有良好的效果。
(二)肿瘤性骨缺损
Biau等[7]报告应用Masquelet技术成功修复1例12岁男孩右股骨尤文肉瘤切除后导致的骨缺损,缺损长度为16 cm,术前术后均予以化疗,术后愈合良好,随访3年后患者髋膝关节活动正常。Chotel等[8]采用Masquelet技术治疗了8例长骨骨肿瘤切除后的骨缺损,缺损长度10~22 cm,一期利用钢板或髓内钉固定,二期植骨治疗,其中7例术前及术后辅助化疗;结果显示除1例未愈合外,其余7例均获得愈合,平均愈合时间4.8个月。Villemagne等[9]报告12例儿童肢体肿瘤,肿瘤切除术后均应用Masquelet技术修复缺损并辅助化疗,其中2例增加放疗治疗,术后平均随访6.2年,肿瘤无复发,11例下肢肿瘤患儿于植骨后平均4.1个月可负重,7例发生骨不连,Villemagne指出通过延长内固定时间可以降低骨不连机率,Masquelet技术为治疗小儿肿瘤提供了一种简单、可靠的方法。
(三)感染性骨缺损
Wu等[10]报告利用Masquelet技术成功治疗36例Cierny-Mader(C-M)Ⅳ型慢性骨髓炎伴骨缺损患者,平均缺损长度5.5 cm(范围,2~10.9 cm),最终所有患者均获得骨愈合,平均愈合时间29.5个月(范围,24~45个月),其中35例(97%)患者骨髓炎得以根治,35例(97%)患者能独立行走,31例(86%)患者恢复工作;作者认为骨愈合与骨缺损的长度无关,而与感染的部位(P=0.005)及患者的年龄(P=0.005)有关。Powerski等[11]报告1例13岁女孩右桡骨骨折髓内钉固定术后感染,采用Masquelet技术彻底清除脓肿及病灶,植入抗生素骨水泥后钢板固定,4个月后二期植骨,植骨3个月后骨缺损获得临床愈合,肘关节屈伸活动良好。Scholz等[12]应用Masquelet技术治疗8例骨缺损伴感染患者,骨缺损长度5.5~14.5 cm,所有患者均采用规范的治疗方案,包括应用抗生素、软组织彻底清创、切除感染骨段及应用外固定架固定骨缺损,在行Masquelet技术前平均进行了4.7次手术;Masquelet术后24个月所有骨缺损均愈合且患肢功能良好。
(四)先天性假关节
Pannier等[13]利用Masquelet技术成功治疗5例胫骨先天性假关节患者,术中切除假关节,骨缺损处置入骨水泥,髓内钉固定,2个月后植入自体髂骨,患肢不负重状态下予以石膏固定2个月;之后更换石膏,负重状态下固定2个月;石膏固定4个月后拆除,辅以腿部支具,所有患者均可自由活动且未发生感染;2例患者因髓内钉固定不良导致小腿畸形,其中1例在随访后的3.5年发生无移位骨折,采用负重状态下石膏固定45 d后治愈。Mansour和Ghanem[14]报告4例胫腓骨先天性假关节患者(其中1例男孩患有左腓骨先天性假关节伴左踝严重外翻畸形);切除假关节后,采用Masquelet技术治疗,8周后取自体髂骨植骨;患者1个月后均可部分负重,1年后接受左踝内翻截骨术,术后植骨愈合,且踝关节功能良好。
二、诱导膜的作用机制
马信龙等[15]通过实验发现在骨缺损中,由于骨折空间扩大,血管内皮生长因子(vascular endothelial growth factor, VEGF)表达所需要的低氧微环境改变,导致VEGF减少,骨修复所需要的新生血管生成不足。这是骨缺损不愈合的重要原因之一。同时实验还发现转化生长因子-β1(transforming growth factor,TGF-β1)与VEGF表达呈正相关,即TGF-β1强表达时,VEGF表达程度也增强,TGF-β1弱表达时,VEGF表达程度也减弱。
诱导膜能够分泌VEGF、TGF-β1、骨形态发生蛋白(bone morphogenetic protein,BMP)-2和血小板内皮细胞黏附分子等多种成骨生长因子、血管生成相关因子[16],因此诱导膜在植骨血管化和成骨修复中具有重要作用。有学者通过实验观察到大量的破骨细胞出现在PMMA附近,考虑破骨前体细胞通过VEGF形成的血管网转运至诱导膜周围[17]。另外,诱导膜还能分泌血管性血友病因子及炎性因子——白细胞介素(interleukin,IL)-6、IL-8等,但这些炎性因子并不影响正常的成骨活动[18]。诱导膜的存在形成了一个独立的空间,将缺损内部的植骨与外界环境隔离,避免了植骨后的吸收现象,诱导膜还将纤维组织和脂肪组织阻挡在骨缺损外,避免周围组织填充于骨缺损处。因此,诱导膜的出现为骨缺损提供了一个稳定的生物学环境。有动物实验显示,在诱导膜内植骨6个月后,新生骨的组织学结构与原本骨结构并无区别[19,20]。
三、Masquelet技术的影响因素
(一)彻底清创
对于外伤导致的骨缺损,坏死组织易诱发感染,所以需要彻底清除骨缺损部位的坏死组织及异物(图1A),同时判断骨质的血运(利用电钻在骨质上钻孔,观察骨质是否出血,即红辣椒征)。去除死骨时应使用低能量截骨工具(如骨刀),以免产生过高的热量灼伤正常骨质[21]。对于非感染性骨缺损,如肿瘤性骨缺损、先天性假关节,需要彻底清除异常骨质,保证后期达到正常的骨愈合。
(二)保持稳定的力学环境
彻底清创后,可以使用单边或环形外固定器、钢板、髓内钉等固定器械,实现局部力学环境的稳定,同时保证骨缺损两端无缩短、旋转及成角畸形。固定器械的选择主要依据缺损的位置:①长骨中段缺损,对于非感染性骨缺损,可直接置入髓内钉;而感染性骨缺损需一期利用外固定架固定(图1B),待感染消除后再予以髓内钉固定(图1C)。因为髓内钉既能保证及维持力线稳定,又能实现患者早期负重。由于髓腔内置入异物,可能会诱发感染,因此暴露在骨缺损的髓内钉外表面可以包裹抗生素骨水泥。髓内钉的存在不会影响诱导膜形成[22],而且由于髓内钉占据骨缺损的空间,能够减少植骨材料的使用[23]。②前臂缺损,可利用钢板和螺钉固定,术中将骨水泥固定在钢板上以防止其移位,避免骨水泥向周围偏移[24]。③邻近关节的缺损,优先使用外固定。环形外固定不但能保持稳定,而且还能在术后调整缺损两端使其无成角。但放置外固定时必须注意穿针点必须远离感染区域。④较小骨骼的骨缺损(如跖骨)或稳定性较好的部分骨缺损,术后采用石膏固定[23]。
(三)骨水泥
骨折稳定后将骨水泥填充于骨缺损中。传统的骨水泥材料是聚甲基丙烯酸甲酯(PMMA)。骨水泥应当充分包绕骨缺损的断端[3],促使形成足够多的诱导膜(图1D),保证后期的植骨不被吸收[25]。填充骨水泥时应使用生理盐水冲洗降温,以防止骨水泥产生的热量灼伤骨质及周围软组织。当治疗胫骨干的骨缺损时,骨水泥应尽可能地接触腓骨,确保形成一个足够坚强的诱导膜环境[26]。对于骨水泥的形态,使用骨水泥垫片优于骨水泥珠,因为骨水泥珠诱导的生物膜不规则,不利于下一步手术。李海峰等[27]依据骨缺损的大小制作出多个骨水泥柱状结构填充物放置于骨缺损部位,结果显示由于填充物较大,便于取出及冲洗,且不会破坏诱导膜和损伤骨-骨水泥界面的骨组织,故修复骨缺损效果较好。
除PMMA外,很多学者对其他能诱导生物膜形成的材料也进行了大量实验研究。硫酸钙作为填充材料填充于骨缺损时具有能被完全吸收的特性,最终无残留,不会成为细菌的病灶引发感染,是一种非常具有前景的材料。Ma等[28]通过动物实验对硫酸钙及PMMA诱导形成的生物膜进行对比,实验结果显示硫酸钙诱导形成的生物膜的骨诱导能力远高于PMMA,因此建议在硫酸钙成骨活性的高峰期(约6周)时取出PMMA,植入硫酸钙来实现最大限度的骨愈合。McConoughey等[29]通过实验,以抗生素洗脱为特征,对含有相同抗生素的硫酸钙和PMMA链珠进行检测,并对其结构进行分析,结果表明作为抗生素的载体抑制细菌时,硫酸钙链珠的效果等同于甚至高于PMMA链珠的效果。魏富达等[30]通过动物实验对PMMA骨水泥与磷酸钙骨水泥诱导的生物膜的结构和成骨活性的差异进行比较,结果发现PMMA骨水泥诱导形成的生物膜较磷酸钙骨水泥具有更强的促血管化和成骨活性。
(四)抗生素
对于开放性骨折,为控制感染,骨水泥也可以与抗生素混合使用,以此提高抗生素局部浓度。Shah等[31]将克林霉素与PMMA混合,通过实验发现局部应用克林霉素既能有效控制感染,还可以恢复炎性细胞因子和生长因子的表达、影响局部组织重建。由于骨水泥聚合反应会产生热量,所以选用的抗生素必须具有热稳定性。氨基糖苷类(庆大霉素、妥布霉素)及万古霉素是很好的选择,它们热稳定性高、洗脱率高、抗菌谱广及过敏性反应发生率低[32,33]。Chang等[34]通过实验证实了在众多加入骨水泥的抗生素中,庆大霉素与万古霉素、替考拉宁、头孢他啶、亚胺培南、哌拉西林、妥布霉素相比,具有最长的洗脱期。由于骨水泥混合抗生素会降低骨水泥的强度[35],且高浓度的抗生素可能会阻碍骨水泥成型[36],所以骨水泥与抗生素混合的最大比例是每40 g骨水泥中加入8 g抗生素。然而,张强等[37]证实在40 g骨水泥中加入抗生素超过4 g后,骨水泥的黏度明显降低,出现成团困难,因此作者推荐抗生素的使用不能超过4 g。
(五)关闭创面
第一阶段的最后一步要求无张力关闭创面。若创面较大难以闭合,可利用皮瓣覆盖创面,但皮瓣转移会增加对周围软组织的创伤。Masquelet[38]对35例长骨缺损患者使用Masquelet技术治疗,其中28例需行软组织修复,包括游离肌瓣14例、带蒂皮瓣11例、筋膜皮瓣3例,虽然3例行筋膜皮瓣修复者出现皮瓣坏死,但28例患者在平均8.5个月的时间里均可在无保护下负重;最终35例患者骨缺损均完全愈合,无一例出现再感染。
(六)植骨
植骨前必须确认感染已得到彻底控制,通常采用观察急性炎症指标的趋势水平(包括红细胞沉降率及C反应蛋白等)进行判断[21]。一般在第一阶段过后6~8周,在保留诱导膜的基础上移除骨水泥,然后向缺损部位植入1~2 mm3的松质骨。术中做纵行切口,利用骨刀小心取出骨水泥(图1E),避免损伤诱导膜;骨水泥取出后,仔细冲洗诱导膜以去除残留骨水泥,而后在缺损部位充分植骨,待植骨与周围骨质融合后骨缺损即修复(图1F)。Luangphakdy等[39]在大动物实验中发现植骨前搔刮诱导膜的内表面,并去除约1~2 mm的诱导膜能够改善植骨后骨重建。植骨后使用可吸收缝线尽量缝合诱导膜,若诱导膜缺损,可利用周围筋膜封闭植骨材料[23]。植骨所需的自体骨可从髂骨、胫骨近端或跟骨通过钻孔-灌洗-抽吸系统(RIA)获得。使用RIA系统获得的自体骨含有骨母细胞及细胞生长因子能够加速骨修复[40,41]。如果自体骨数量不足,可在自体骨中加入脱钙的异体骨。植骨时异体骨与自体骨的比例一般不超过1∶3[42],但Karger等[3]认为比例为1∶1时也可以获得良好的骨愈合。同种异体松质骨、脱钙骨基质均具有较好的骨传导性及骨诱导能力,有学者分别采用海绵状及泥灰状脱钙骨基质修复骨缺损进行实验研究,结果表明两种脱钙骨基质均具有较强的成骨能力,泥灰状脱钙骨基质颗粒细小,流动性好,适用于囊性骨缺损的微创治疗;而海绵状脱钙骨基质成骨质量高,可广泛用于植骨融合术和骨缺损的治疗[43]。
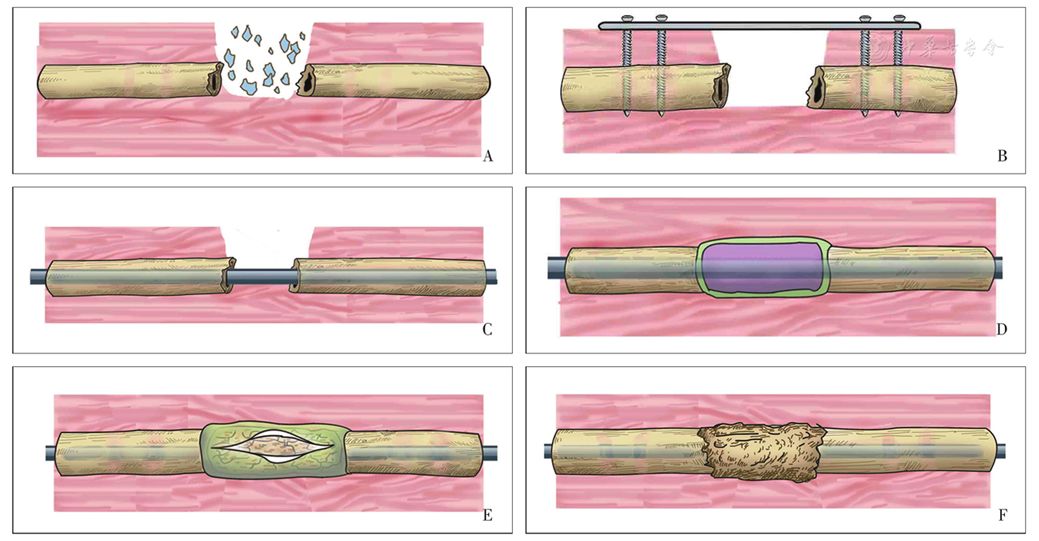
图2 Masquelet技术手术操作示意图 A 开放性骨折,污染严重,可见骨缺损 B 清创后予以外固定架临时固定,等待感染消除 C 彻底清创后,置入髓内钉,保持稳定的力学环境 D 将骨水泥置于骨缺损中,骨水泥包绕骨缺损的断端,6~8周后形成诱导膜 E 第一阶段进行6~8周后,在保留诱导膜的基础上移除骨水泥垫片并在缺损部位植骨 F 植骨与周围骨质融合,骨缺损修复
其他材料也可以用于骨缺损的治疗,如磷酸三钙、钛微球复合材料等,但结合膜诱导技术的案例并不多。有研究表明向自体骨中添加骨形态发生蛋白、唑来膦酸等能够增强骨愈合能力[44]。张一等[45]将抗生素硫酸钙颗粒填充于骨缺损处,对较大的骨缺损可同时取髂骨植骨,术后所有患者骨缺损均愈合,作者指出在骨缺损长度
四、Masquelet技术与其他技术比较
目前,修复四肢骨缺损的方法包括Ilizarove骨搬移技术、自体骨松质骨植骨、带血管腓骨移植技术等。Ilizarove技术适应证广泛,尤其适用于伴有软组织缺损及感染的患者,但该技术操作复杂,对术者技术要求高,同时存在延长骨力线偏移、钉道感染、截骨端封闭过早或瘢痕填充影响对接端愈合等并发症,而且当骨缺损超过8 cm时,再骨折风险明显增高[46]。带血管蒂骨移植愈合较快,但需要显微操作技术,且并发症较多,如受区并发症包括应力性骨折、感染、骨愈合不良等;供区并发症包括自发性骨折、关节不稳、伸肌腱挛缩甚至骨筋膜室综合征等[47]。而同种异体骨移植存在异物排斥反应、感染率高、疾病传播等风险。
与其他技术相比,Masquelet技术具有操作简单、安全、并发症少、易于被患者接受和临床推广等优点,适用于各部位骨缺损,临床应用潜力大。Masquelet技术特别适用于其他治疗手段无效的大段骨缺损。El-latief等[48]将30例胫骨缺损超过4 cm的患者,分为A、B两组,A组15例患者采用Masquelet技术进行治疗,B组15例患者采用Ilizarove技术进行治疗。通过对比,El-latief认为与Ilizarove技术相比,Masquelet技术具有以下优点:①在无需行复杂的软组织修复重建术的前提下,其操作简单;②对患者要求不高,相比于Ilizarove技术,患者本人术后无需对外固定进行调整;③治疗较大的骨缺损时所需时间较短。但Masquelet技术需要有良好的局部条件,即放置抗生素骨水泥2个月后未发生感染或感染已得到控制,局部软组织条件良好,才可进行植骨,且该技术对已存在肢体短缩的患者无法恢复其肢体长度。Tong等[49]对39例创伤后骨髓炎的患者分别利用Masquelet技术(20例)与Ilizarove技术(19例)进行治疗,术后两组患者均取得满意结果,其中使用Masquelet技术治疗者术后有17例(85%)功能达到良好,而使用Ilizarove技术治疗者术后有9例(47%)功能达到良好,两者比较差异有统计学意义(P=0.017)。因此,作者认为在股骨骨髓炎治疗中,Masquelet技术较Ilizarove技术可以获得更好的结果。
总之,Masquelet技术操作简单、安全、并发症少、对受区要求低、易于被患者接受和临床推广,适用于各部位骨缺损,特别是其他治疗方法无效的大段骨缺损治疗。但该方法仍存在许多问题需要进一步研究。例如,选择哪种材料(如使用PMMA骨水泥,则成膜后需要将其取出;而使用可吸收的硫酸钙诱导成膜,则价格昂贵)来诱导具有生物活性的诱导膜,在植骨材料中添加哪些物质能有效提高骨愈合等。相信随着研究的不断深入,这些问题终将被逐一解决。
参考文献(略)
继《回来的女儿》后,迷雾剧场又推出四部大剧,有你期待的吗?
#头条创作挑战赛#2022年12月,迷雾剧场推出的悬疑剧《回来的女儿》,斩获了不错的口碑和收视,剧情、人物设定都很不错,每个人都有嫌疑,看得观众热血沸腾。张子枫、梅婷、王砚辉三位主演的表现,那可是相当出彩,小细节处理到位,表演生动自然,引发了观众的强烈共鸣。继《回来的女儿》后,迷雾剧场又推出四部悬疑大剧,一起来看看有没有你期待的!第一部:《尘封十三载》娱乐天地2023-05-27 01:54:520000“最红裸模”张筱雨:22岁时拍写真火爆全网,如今将近40岁仍单身
文编|史争旦夕看生活百态,品人世间味道,在阅读文章之前,您可以先动动小手点个关注点个赞!1985年,张筱雨出生在哈尔滨一个小村庄中,她的父母都是农民,过着面朝黄土背朝天的生活,即便如此,父母还是非常爱她,尽自己所能给她想要的东西。张筱雨是一个非常聪明的孩子,学习知识的时候一点就通,就连老师都经常夸奖她。娱乐天地2023-09-23 16:05:460007于正力捧的美女演员,撞脸安以轩,如今26岁演《以家人之名》获赞
说起何瑞贤,很多人并不熟悉,毕竟她还算个新人演员,但其实她本人非常的优秀,不仅在2012年以专业第一名的成绩被北电录取,还被知名编剧于正欣赏,在公众平台上发文,夸奖她试戏的表现非常优秀,并于2018年正式签约到旗下。娱乐天地2023-05-20 09:23:310000这是曾经霸气的希拉里?和克林顿海边度假身材发福严重,皮肤松弛
希拉里和克林顿,这对年过七旬的夫妇,如今已过了风光的政坛岁月,安然享受着晚年生活的宁静。时光无情地在他们脸上刻下了岁月的痕迹,年轻时的风采已经难觅踪影。曾经闪耀在舞台上的希拉里,如今显得有些风光不再,尤其是她素颜亮相时,那张松垮的脸庞已经不再是当年的霸气感了。娱乐天地2023-11-09 15:58:270000华人电影现役男演员排名,成龙与李连杰是泰山与北斗,周润发呢?
香港电影在九十年代走入最辉煌的时代,也是从这个时候开始,成龙和李连杰正式成为华语电影的领军人物,并且将香港电影带给了全世界的观众。李小龙是世界著名的武术家,全世界最受欢迎的华人功夫巨星,他的历史地位自然毋庸置疑,一直以来都是华人电影的标杆人物。李小龙之后最杰出的男演员无疑是成龙和李连杰了,这两人不仅是华人功夫界的泰山北斗,更是我国当代电影界的灵魂人物,两人之后再无有如此影响力的巨星出现。娱乐天地2023-07-27 11:06:460000

 正在请求数据,请稍候!
正在请求数据,请稍候!




